
Understanding Tradition
Mastering Innovation
テーパーウェッジ型のコンセプトを持つ大腿骨ステムは、短・中・長期いずれにおいても優れた安定性を得られることがさまざまな臨床研究により明らかにされています[1,2,3]。
MasterLoc Hip Systemはこの理念を追求し、初期の安定性と長期固定力を兼ね備えたMectagripコーティングを採用しています。
最適化されたデザインにより、MasterLoc Hip SystemはAMISアプローチをはじめ、あらゆるMIS手技での使用が可能となっています。

真空下プラズマスプレー法(VPS)で溶射された純チタンのコーティング層は、初期固定を得るために高い摩擦係数[4]をもち、ボーンイングロースを促進するよう設定された気孔(連通性をもつ100~350μm)により、長期的な固定性[5,6,7,8]も期待できます。

MasterLoc Hip SystemはあらゆるMISアプローチに適合するように設計されています。手術器械とインプラントは、AMISアプローチをはじめとする、MISアプローチを用いた場合でも軟部組織を損傷するリスクを軽減する特別な設計となっています。


このステムは大腿骨髄腔に挿入されたステムが、自然と正しい位置に導かれ内外側方向での安定性を得られるように設計されています。
骨温存をはかるため、MasterLoc Hip Systemは遠位部をリデュースし、ステム長を短くしています。
この特徴により、髄腔形状を問わず、Dorr Type A、B、Cどのタイプにも、骨幹端での最適な髄腔適合性を得ることが期待できます。初期のテーパーウェッジ型ステムに見られた、遠位固定に代表される髄腔との不適合の問題を減少することができます[9]。
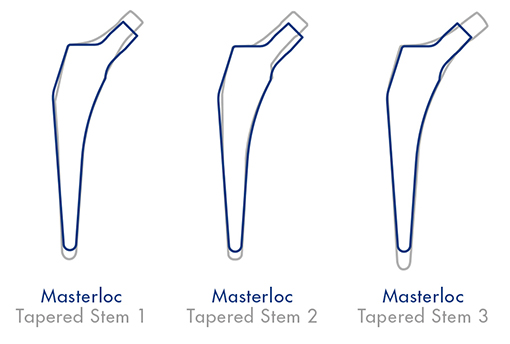
MasterLocのサイズバリエーションは以下の通りです:
ラテラライズドタイプは脚長を維持しつつ、6mmのラテラルオフセットを追加できます。
チタン合金
MasterLoc Hip Systemはチタン合金製(Ti-6Al-7Nb、ISO 5832-11)です。この材料は高い弾性係数と生体適合性を持つことで知られています[10]。
MECTAGRIP COATING
MasterLoc Hip Systemの大きな特徴のひとつがMectagripコーティングです。
Mectagripは高い摩擦係数による初期の安定性と、チタンプラズマ溶射の特有の良好な長期成績を享受できるよう設計された、Medacta独自のプラズマ溶射チタンコーティングです[11]。プラズマ溶射コーティングは、セメントレス人工股関節置換術において、その確実な固定性により高い臨床成績を誇る表面処理のひとつとなっています。1980年代に導入されて以降、セメントレス固定におけるゴールドスタンダードのひとつとなっています[12]。
Mectagripは真空プラズマ溶射法(VPS)で溶射された純チタンにより層が形成されます。このチタンコーティングに用いられたVPS法にはたくさんのメリットがあると考えられます。
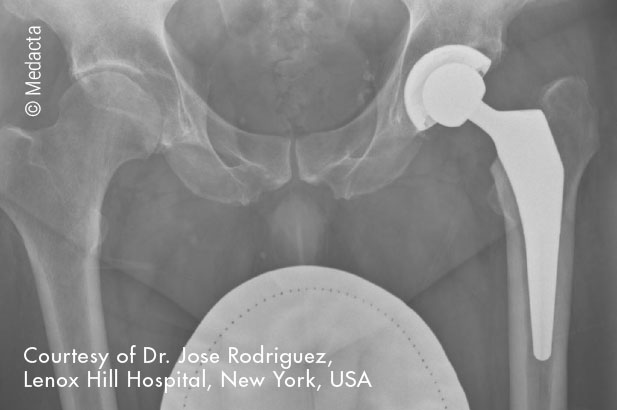
遠位部をリデュースさせたテーパーウエッジ型ステム
MasterLoc ヒップシステムのデザインコンセプトはM. E. Müller先生によって提唱された基本コンセプトを踏襲しています。

TAPERED WEDGE DESIGN
MasterLoc Hip Systemは髄腔骨幹端内で内外側面でしっかりした安定を得るためにA/P面に3°テーパーを採用しています。近位部で髄腔占拠率を高め、遠位をリデュースさせたことで、遠位固定の危険性を減少させました.
Wolffの法則によると、負荷をかけられた骨の骨密度は増大します[13]。ステム近位部で良好な荷重伝達を維持する事で、骨幹端において良好な骨質を維持することが可能となります。
リデュースさせた遠位形状
第1世代のテーパーウエッジ型ステムでは、高いサイペインの発生率が様々な研究で報告されています。これは特定の患者の解剖学的形状(主にDorr Type Aの髄腔)において発生した、遠位固定に起因しているものと考えられています[14]。第2世代のテーパーウエッジ型ステムは遠位部をリデュースすることによって、この問題に対応しています[15]。
MasterLoc Hip Systemは遠位がリデュースされていることが特徴で、近位骨幹端の髄腔占拠率を高めます。Dorr type Aの髄腔にも適したものとなっており、同時に骨温存を可能にします。
MIRROR POLISHED NECK WITH REDUCED A/P GEOMETRY
ネック部分に鏡面仕上げを施すことにより、軟部組織への損傷やライナーの摩耗を最小限に抑えます。
さらに、ネック前後径をリデュースすることで広い可動域を確保しました。

前方アプローチは、筋間・神経間を通り股関節に到達する唯一のアプローチで、股関節周辺の筋肉、腱、血管、神経への損傷のリスクを軽減でき、その良好な治療成績は長年の臨床経験から実証されています。
AMISアプローチはMedactaのサポートのもと、経験豊富な世界規模の整形外科医グループによって2004年に開発されました。従来の前方アプローチの特徴に加えて、その再現性を高め、軟部組織への侵襲を更に抑えることが期待できるアプローチとなっています。
Medacta Internationalは、AMIS(前方最小侵襲手術)の導入・改善を目指す整形外科医の研修プログラムを世界各地で実施しております。世界各地に設立されているリファレンスセンターでの手術見学を通じてAMISをより深く理解して頂くことができますし、必要に応じて継続的な研修プログラムも御提案させて頂きます。また、手術器械もAMISアプローチにより特化したものへ日夜、研究、改良を続けております。
MasterLoc Hip SystemはMedacta InternationalによるAMISの世界への入り口となります。

Discover:
AMIS モバイルレッグポジショナーはAMIS器具システムの構成要素として提供されるもので、手術中の肢位の変更と保持を確実で効率よく実施することが可能となります。牽引、外旋、過伸展、内転など、AMISアプローチに必要な下肢の操作が容易に行えます。
[1] Healy W, Tilzey J, Lorio R, Specht L, Sharma S. Prospective, Randomized Comparison of Cobalt-Chrome and Titanium Trilock Femoral Stems. J Arthroplasty. 2009;24:831-6.
[2] Parvizi J, Keisu K, Hozack W, Sharkey P, Rothman R. Primary total hip arthroplasty with an uncemented femoral component: a long-term study of the Taperloc stem. J Arthroplasty. 2004 Feb;19(2):151-6.
[3] McLaughlin J, Lee K. Total hip arthroplasty with an uncemented tapered femoral component. J Bone Joint Surg Am. 2008 Jun;90(6):1290-6.
[4] Friction testing of the Mpact and Versafitcup coating samples. Data on file Medacta.
[5] P. Robotti, A. Sabbioni, L. Glass, B. George, Macroporous Titanium Coatings , by Thermal Plasma Spray, ITSC 2013, International Thermal Spray Conference, May 13 –15, 2013,Busan, Korea.
[6] J. E. Biemond et al, In vivo Assessment of Bone Ingrowth Potential of 3-Dimensional E-Beam Produced Implant Surfaces and the Effect of Additional Treatments by Acid-Etching and Hydroxyapatite Coating, J. Biomat. Appl, published on line January 27, 2011, 0885328210391495.
[7] De Godoy RF, Blunn G, Coathlup ML, Goodship AE. In vivo Evaluation of Titanium Macro-Porous Structures Manufactured Through an Innovative Powder Metallurgy Approach. Proceedings eCM XIII: Bone Fixation, Repair & Regeneration, June 24–26, 2012, Davos, Switzerland.
[8] Goodshi A, Blunn G, Preve E, Facchini L, Bucciotti F, Robotti P. In-vivo Assessment of the Ingrowth Potential of Engineered Surface Topographies Produced by Spark Plasma Sintering. Proceedings 9th World Biomaterial Congress, June 1-5, 2012, Chengdu, China.
[9] McLaughlin JR, Lee KR. Cementless total hip replacement using second-generation components: a 12- to 16-year follow-up. J Bone Joint Surg Br. 2010 Dec;92(12):1636-41.
[10] Khan W, Muntimadugu E, Jaffe M, Domb AJ (2014). Implantable Medical Devices In W Khan and AJ Domb, Focal Controlled Drug Delivery (p. 33-59). Springer New York Heidelberg Dordrecht London.
[11] Khanuja HS, Vakil JJ, Goddard MS, Mont MA. Cementless Femoral Fixation in Total Hip Arthroplasty. J Bone Joint Surg Am. 2011;93:500-9.
[12] Lombardi AV. Porous, plasma-sprayed, titanium-tapered cementless stems achieve versatility. Orthopedics Today, June 2006.
[13] Wolff J. Das Gesetz der Transformation der Knochen. A Hirschwald, Berlin, 1982.
[14] Cooper H, Jacob A, Rodriguez J. Distal Fixation of Proximally Coated Tapered Stems May Predispose to a Failure of Osteointgration. J Arthroplasty. 2011;26:78-83.
[15] McLaughlin JR, Lee KR. Cementless total hip replacement using second-generation components: a 12- to 16-year follow-up. J Bone Joint Surg Br. 2010 Dec;92(12):1636-41.